Příručky - krmiva psů a koček
8. Specifita nutričních požadavků psů a koček trpících GIT poruchami
Specifita nutričních požadavků psů a koček trpících GIT poruchami
Onemocnění periodontu
Mezi nejčastější onemocnění postihující dutinu ústní psa a kočky můžeme bezesporu zařadit onemocnění periodontální (60-80%). Jsou to plakem podmíněná zánětlivá onemocnění. Nejdříve dochází k rozvoji gingivitidy, zánětu dásní, což je vratný proces. Nebude – li však zahájena patřičná terapie proces progreduje až k onemocnění peridontu.
Infekce periodontu je spojována se zvýšenými hladinami C-reaktivního proteinu, prozánětlivých cytokinů, cholesterolu, plazmatického fibrinogenu, bílých krvinek a krevní glukózy. Malá, toy a brachycephalická plemena jsou více náchylná na různé vady skusu, což zvyšuje riziko pro akumulaci zubního plaku. Navíc jsou brachycephalická plemena predisponována k dýchání ústy, tudíž dochází k neustálému zvlhčování a iritaci orální sliznice. Nemoci peridontu, resorpce zubu a gingivostomatitida jsou četnější u čistokrevných plemen koček, zejména asijských plemen. Věk zvyšuje náchylnost k onemocnění u psů i koček.
Etiologie
Úvodní fáze tvorby plaku je tvořena formací zubního povlaku – pelikuly. Pelikula je tvořena z glykoproteinů a proteinů pocházejících ze slin a tekutiny dásní. Začíná se formovat na čistém zubním povrchu během několika minut. Tato tenká vrstva ulpívá na povrchu zubu převážně elektrostatickými silami mezi negativně nabitými fosfátovými skupinami v molekule hydroxyapatitu a pozitivně nabitými složkami slin a tkáňové tekutiny v dásních. Z počátku pelikula chrání a lubrikuje povrch zubu. Avšak debris a plak tvořící bakterie, které jsou běžnou součástí dutiny ústní, začínají velmi rychle adherovat na pelikuly a množit se. Během 24 hodin pokrývá hladká vrstva plaku celý zub. Nově tvořený plak je měkká, želatinozní hmota tvořená bakteriemi, jejich metabolickými produkty, detritem a složkami slin. Nejsilnější vrstva se usazuje u dásně na bázi zubu. Důvodem je to, že zde nedochází k samovolnému čištění při mastikaci. Pokud ponecháme aerobní a fakultativně anaerobní bakterie volně množit, vrstva plaku postupně zesiluje a stává se obtížněji slupitelnou z povrchu zubu. Nejčastější bakteriální původci jsou G+ fakultativní patogeny jako Actinomyces sp, Streptoccocus sp. U psů jsou navíc často nacházeny Porphyromonas: P. gluae, P. salivosa a P. denticans.
Zubní plak slouží jako organická matrix pro následnou mineralizaci. Precipitace minerálních solí nastupuje do dvou týdnů od vytvoření plaku. Zubní kámen je drsná, porovitá struktura, pokrývající povrch zubu. Je tvořen ve vrstvách. U psů se v něm často nachází chlupy a zbytky potravy. Minerální látky tvořící supragingivální zubní kámen pochází ze slin, subgingivální plak je tvořen z minerálů tkáňové tekutiny. Nejčastěji se jedná o uhličitan vápenatý a fosforečnan vápenatý. Zubní kámen není sám o sobě považován za patologické agens. Udržuje však plak v kontaktu s dásní což přispívá k iritaci sliznice a narušuje samočisticí schopnost zubu.
Gingivitida je způsobena supragingiválním plakem. Kontakt plaku a sliznice vede k jejímu poškození a následně k zánětlivé odpovědi organismu. Rozšiřováním plaku (subgingivální plak) pod sliznici dásně vede ke vzniku dásňového sulku. Pokud tento stav nebude léčen, dochází k progresi procesu v tzv. periodontální kapsu. Substance, která se nachází v této kapse je tvořena neadherovaným plakem a bakteriemi. Jsou to především G+,fakultativní druhy a některé druhy G-. Jelikož tyto bakterie utilizují kyslík, podporují tím růst anaerobních bakterií.
Onemocnění peridontu se rozvine pokud vystavíme periodontální vazy účinkům plaku, bakterií a bakteriálním produktům. Je to tedy plakem vyvolané, progresivní zánětlivé onemocnění postihující dáseň, pojivou tkáň mezi kořenem zubu a zubní jamkou a alveolární kost. Podpůrná pojivová tkáň a okolní kosti slábnou a může dojít ke ztrátě zubů. Onemocnění peridontu jako takové vede k diskomfortu a bolesti. Pokud není léčeno může dojít k proniknutí bakterií do krve a rozvoji vážnějších zdravotních komplikací například k bakteriální endokarditidě. Bylo zjištěno, že psi s vážnými příznaky onemocnění měli po žvýkání žrádla zvýšené množství bakterií v krvi.
Mezi hlavní klinické příznaky můžeme zařadit zápach z úst, krvácející, zarudlé dásně, ztrátu zubů a potíže s příjmem potravy spojené s bolestivostí a ulcerace na sliznici.
Prevence
Jako nejúčinnější prevenci doporučují veterinární lékaři čištění zubů kartáčkem každý den nebo každý druhý den. Čištění je vhodné spojit s nějakým příjemným prožitkem (například posledním večerní procházkou). Jako vhodný kartáček je nejjemnější kartáček značky Curaprox. Hlavici se štětinami je třeba po namočení do horké vody vytvarovat. Používáme dětskou zubní pastu nebo speciální pastu pro psy na čištění zubů.
Pokud není čištění zubů možné lze využít tyto prostředky:
- výplachy dutiny ústní (např. MaxiGuard Oral Cleansing Spray or CET Oral Hygiene Rinse).
- dentální ubrousky (Detacetic wipes)
- aditiva do pitné vody ((Biotene nebo Petrodex)
- antimikrobiální agens jako chlorhexidine digluconate
Některá krmiva pro psy a kočky byla navržena, aby usnadňovala odstraňování plaku ze zvířecích zubů. Veterinary Oral Health Council (VOHC) poskytuje seznam produktů u kterých bylo prokázáno pomalejší tvoření plaku nebo zubního kamene. viz http://www.vohc.org/accepted_products.htm
Role krmiva na rozvoji onemocnění
Mokré, konzervované nebo měkké doma připravované krmivo je méně efektivní než krmivo suché. Avšak krmení suchým krmivem samo o sobě nemůže předcházet rozvoji onemocnění. Suché krmivo musí splňovat určité parametry, aby byla mechanická očista co nejlepší. Na prvním místě je to velikost částic. Tyto částice musí být dostatečně velké, aby u psa vyvolaly reflex kousání. Tvar musí být takový, aby došlo alespoň částečně k průniku zubu do částice a tím pádem k očištění zubu. Navíc se nesmí částice po skousnutí okamžitě rozdrtit na menší kousky. Důležitým faktorem je jak dlouhou dobu stráví pes žvýkáním. Rozlišujeme pomalé a rychlé žvýkače. Určitou roli hraje také frekvence podávání žvýkacích hraček a pamlsků. U těchto předmětů hraje roli jejich elasticita a odolnost. Svými vlastnostmi usnadňují mechanickou očistu celého povrchu zubu a výrazně prodlužují dobu žvýkání. Často se používají v kombinaci právě s chemickými látkami, jako solemi polyfosfátů nebo chlorhedinem. Soli polyfosfátů vyvazují vápenaté ionty slin a tím zabraňují tvorbě zubního kamene. Kromě solí polyfosfátů se používají ještě další látky, které zabraňují tvorbě zubního kamene popřípadě mají bakteriostatický efekt. Je to epigallocatechin gallát (catechin) patřící mezi polyfenoly. Jeho zdrojem je zelený čaj. Vyznačuje se antibakteriálním působením proti patogenům způsobujících zubní plak. Navíc je to silný antioxidant. Rozpustné soli zinku, jako například zinek askorbát či zinek glukonát se používají na kontrolu zubního plaku u koček. Jsou obsaženy v čistících gelech a výplaších. Rozmarýnový, levandulový a eukalyptový olej se využívají pro snížení zápachu z tlamy, navíc mají schopnost snižovat množství těkavých sirných sloučenin. Eukalyptový olej dokonce inhibuje růst patogenů.
Podávání tvrdých kostí na žvýkání moc nedoporučuji. Kosti se mohou tříštit na ostré části a poranit psa, navíc může kost uvíznout v krku, což je často indikace k chirurgické operaci. Nebo může dojít k vylomení zubů postižených patologickým procesem.
I přesto, že existuje řada chemických prostředků, které nám slibují odstranění kamene a plaku (jako například pasty, spreje, roztoky), nejdůležitější stále zůstává mechanická očista. Tyto prostředky můžeme používat v kombinaci s mechanickým čištěním plus ještě doplnit čištění nějakým žvýkacím pamlskem.
Syndrom GDV - Gastric dilatation and volvolus
Syndrom dilatace a volvolu žaludku je život ohrožující onemocnění psů. Je charakterizováno rychlým a abnormálním roztažením žaludku (dilatace) a často doprovázeno jeho otočením podél dlouhé osy (volvolus). K dilataci dochází v případech kdy se plyn, tekutina a sekrety hromadí v žaludku a nemůžou být vyloučeny dále do trávicího traktu z důvodu uzavření jak pylorického tak kardiálního svěrače. U postiženého psa dochází rychle ke zhoršení kondice. Je to způsobeno tím, že dilatovaný žaludek tlačí na hlavní břišní cévy, portální vénu a zadní dutou žílu. Tento tlak způsobí ztrátu krevního zásobení žaludku a dalších orgánů dutiny břišní. Navíc dochází ke snížení srdečního výdeje a rozvíjí se šok. Srdeční arytmie byly pozorovány u více než 40% psů s GDV. Tyto arytmie mohou způsobit smrt během týdne nebo měsíce po zotavení se ze syndromu GDV. Tímto syndromem jsou často postiženi psi s velkým hlubokým hrudníkem – Svatobernardský pes, Irský setr, Gordon setr, Královský pudl, Baset a Doga.
Klinické příznaky
Mezi hlavní klinické příznaky patří abdominální bolestivost a dispenze. Dále se objevuje kňučení, salivace a apatie. Zvíře může projevovat pokusy o zvracení, avšak neúspěšně. Jak proces progreduje, začíná se objevovat hypovolemický šok, který se projevuje nitkovitým pulsem, bledými sliznicemi, zrychlenou srdeční činností a unaveností.
Terapie
Jedinou možností terapie je operace – provede se dekomprese žaludku a jeho otočení. Jako preventivní opatření lze provést gastropexi – přišití stěny žaludku ke stěně dutiny břišní. Tento postup zabrání otočení žaludku kolem podélné osy.
Typický rentgenologický nález při GDV 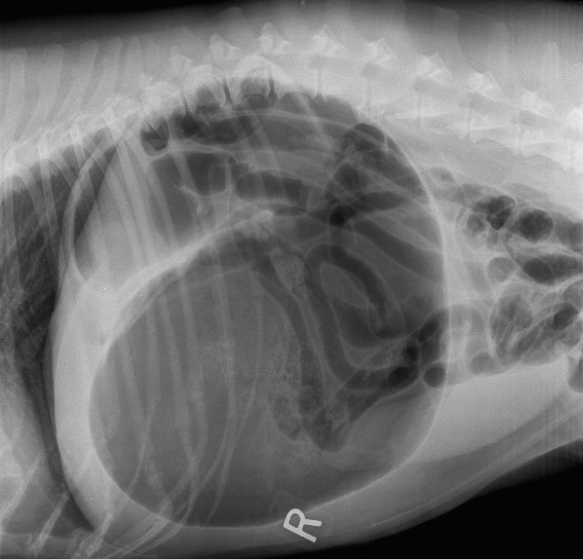
Zdroj: http://www.coolspringsah.com/our-blog/2014/6/18/seriously-scary-gdv
Etiologie
Na rozvoji tohoto faktoru se podílí řada faktorů. Mezi hlavní můžeme zařadit genetickou predispozici, vnitřní abnormality jako zvýšenou hladinu sérového gastrinu nebo porušenou motilitu střev. Gastrin je hormon produkován ve sliznici žaludku a střeva a stimuluje žaludeční sekreci a žaludeční a střevní motilitu. Faktory prostředí jako stres nebo nadměrná excitace zvířete před nebo po krmení, nebo příjmu většího množství vody může přispět k rozvoji GDV. Velký vliv na rozvoji onemocnění má i způsob krmení, typ krmení a jeho složení. Bylo zjištěno, že pokud rostoucí pes dostává krmivo pouze jednou denně, má větší a těžší žaludek, než pes, který dostává krmivo rozděleno do třech stejných dávek. Navíc takový pes krmnou dávku většinou rychle spořádá, přičemž může dojít také k polykání vzduchu. Krmení zbytky ze stolu, podávání pamlsků mezi krmením a přidávání konzervovaného krmiva do běžně krmeného krmiva zvyšují riziko vzniku GDV. Podávání krmiva do vyvýšené misky predisponovaným plemenům nezabrání jejich nafouknutí ba dokonce toto riziko zvyšuje.
Pooperativní péče spočívá v podávání malého množství vody několikrát denně první den po operaci. Pokud je voda tolerována a nedochází k zvracení, můžeme pomalu začít podávat krmivo 6 – 8krát denně. Nejvhodnější je dieta určená pro GIT onemocnění ve formě kaše. Nevyskytují – li se žádné komplikace, v průběhu následujících 3 – 4 dnů navyšujeme postupně krmnou dávku až se dostaneme na dávku před operací.
Prevence
Co se prevence týká, je třeba krmnou dávku rozdělit do několika malých dávek. Tím zamezíme nárazovému přeplnění žaludku psa. Krmení by mělo probíhat v době, kdy můžeme na psa alespoň 1-2 hodiny po nakrmení dohlédnout. Navíc při krmení musíme omezit stres zvířete. Pes by neměl dostat krmení alespoň 1 hodinu před a 3 hodiny po cvičení. Taky je třeba se vyvarovat vypití velkého objemu vody po cvičení nebo po nakrmení.
SIBO/ARD
SIBO- Small intestine bacterial overgrowth/ARD - antibiotic-responsive diarrhea
SIBO/ARD je onemocnění, které se objevuje, pokud dojde ke kvalitativním a kvantitativním změnám v populaci mikroorganismů proximální části tenkého střeva. U psa se jedná především o koliformní druhy bakterií, stafylokoky, enterokoky, Clostridia a Bacteroides. U koček se můžeme setkat s bakteriemi rodu Bacteroides, Pasterella, fusobakterie a eubakterie. Může se rozvinout také sekundárně v souvislosti s jinou patologií střeva (porucha střevní motility, dlouhodobé nebo nadměrné perorální podávání antibiotik nebo antacid, lymfocyto-plasmacitární enteritid, EPI) nebo idiopaticky. Motilita střeva zabraňuje bakteriálnímu přerůstání. Narušení střevní motility může být způsobeno obstrukcí střeva, neuropatií, chirurgickým zákrokem v dutině břišní, peritonitidou, pankreatitidou, urémií, hypokalemií a endotoxemií. Mezi nejčastější klinické příznaky patří občasný průjem doprovázený zvracením nebo nechutenstvím.
Diagnoza
Pro diagnostiku SIBO/ARD můžeme využít jak metody přímé tak nepřímé. Mezi přímé metody patří stanovení počtu bakterií v duodenální tekutině. Jako nepřímé metody diagnostiky můžeme využít stanovení folátů, kobaltaminu a žlučových kyselin ze séra. Hladina folátů bude zvýšená vlivem bakteriální produkce. Můžeme očekávat sníženou hladinu vitamínu B12 (bakterie zabraňují vazbě B12 na vnitřní faktor) a zvýšenou hladinu nekonjugovaných žlučových kyselin (dekonjugace kyselin bakteriálními enzymy).
Pathogen Overgrowth – Bakteriální přerůstání
Mikrobiální populace je velmi náchylná na změny. Její složení může být ovlivněno stresem, infekcí, podáváním antibiotik, nutričními faktory, poruchou motility a imunosupresí. Bakteriální přerůstání se může manifestovat jako samostatné onemocnění nebo jako složka SIBO/ARD nebo jiné forma poškození střeva.
Množící se patogenní baterie produkují toxiny, karcinogeny a hnilobné substance, které mohou přímo poškodit sliznici střeva, způsobit systémové onemocnění a v neposlední řadě inhibovat růst bakterií prospěšných. Nejčastějším střevním patogenem je Klostridium perfringens.
Běžné klinické příznaky zahrnují zvracení, průjem, ztrátu hmotnosti a v některých případech celkové postižení organismu vlivem produkovaných toxinů.
Inflammatory Bowel Disorders - Zánětlivé onemocnění střeva
IBD je multifaktoriální onemocnění. Zahrnuje rozdílnou skupinu poruch, které jsou obvykle klasifikovány podle typu převládajících zánětlivých buněk v mukóze střeva a podle postižené plochy.Nejčastěji bývají diagnostikovány zánětlivá onemocnění tlustého střeva (lymfocytoplasmatický, eosinofilní, histiocytární a granulomatozní zánět).
Chronické idiopatické zánětlivé onemocnění střeva (CILBD) je onemocnění související jednak se stresem a jednak s dalším faktorem, který ovlivňuje funkci střeva. Mezi tyto doprovodné faktory můžeme zařadit zánětlivé onemocnění, potravní intoleranci, bakteriální přerůstání, parazitární infekce a nádorová onemocnění.
Mezi hlavní klinické příznaky patří zvýšená frekvence vylučování, tenesmy a krvavý nebo hlenovitý průjem. Pokud je postiženo i tenké střevo můžeme pozorovat velké množství měkkého a objemného trusu popřípadě průjem s příměsí nestrávených tuků.
Léčba IBD a CILBD:
Při léčbě těchto dvou onemocnění se neobejdeme bez medikace. Cílem terapie je uklidnit zánětem podrážděnou sliznici a napomoci jejímu zahojení. Postiženým zvířatům podáváme protizánětlivé a imunosupresivní látky – kortikosteroidy (PREDNOSON nebo PREDNISOLON), SULFASALAZIN a v některých případech perorálně CYKLOSPORIN nebo METRONIDAZOL.
Tyto látky se vyznačují řadou nežádoucích účinků, proto je vhodné je podávat jen po nezbytně nutnou dobu.
Dietní management nám pomůže udržovat stav v remisi a předcházet možným relapsům onemocnění.
Dietní řešení GIT onemocnění
Dieta, která nám má pomoci zvládnout onemocnění GIT, by měla být vybírána tak, aby ochránila postižený úsek trávicího traktu. U akutně probíhajích onemocnění je vhodné poskytnout postiženému zvířeti krátkodobý půst (12 – 48 hodin) nebo výrazně omezit příjem potravy. Význam těchto opatření je v tom, že poskytneme střevu určitý čas na odpočinek. Déle probíhající onemocnění je třeba zvládnout vhodně zvolenou dietou.
Zdroj proteinů
EPI, SIBO/ARD a některé formy zánětlivého onemocnění střev můžou narušit trávení a vstřebávání proteinů. Může dojít k proteinové malnutrici. PLE (protein losing enteropathy) se objevuje, pokud dojde k rychlé a značné ztrátě proteinů. Pokud proteiny nejsou kompletně stráveny, dostávají se pasáži zažitiny do tlustého střeva, kde jsou metabolizovány bakteriemi kolonu – Bacterides spp a Clostridia spp. Tyto bakterie fermentují polypeptidy a aminokyseliny a začínají se intenzivně množit. Problém je, že zdravá, vyvážená mikroflora střeva je převážně tvořena bakteriemi sacharolytickými (štěpícími cukry).
Proto je důležité zajistit v dietě protein vysoké kvality, dobře stravitelný a nejlépe protein z jednoho zdroje (z důvodů možné hypersenzitivity). Nejlépe je vybrat ten zdroj proteinu, kterému zvíře nebylo dříve exponováno.
IBD může vézt k poruše trávení proteinů a poškodit sliznici střeva. Intaktní proteiny z potravy mají větší možnost dostat se přes poškozenou sliznici do lamina propria a stimulovat imunitní odpověď v aktivní periodě onemocnění. Nový zdroj proteinů, který je krmený během počáteční fáze onemocnění má jen krátkodobý přínos. Za 4 až 6 týdnů dietní terapie je třeba zdroj proteinu změnit a zvolit nějakou udržovací dietu. Bohužel v současné době nejsou žádné klinické ani experimentální důkazy o účinnosti tohoto postupu.
Zdroj cukrů
Při onemocnění GIT je vhodné dietou dodávat hlavně jednoduché cukry, které jsou snadno vstřebatelné a jsou pohotovým zdrojem energie. Jako vhodný zdroj cukrů můžeme doporučit bílou rýži, brambory, tapioka a kukuřice. Bramborový a tapiokový škrob je méně stravitelný než rýžový. Kukuřice může být kontraindikována u zvířat, která jsou na tuto složku krmiva alergická. Pšenice, oves a ječmen obsahují gluten. Gluten je zásobní protein, který s vodou tvoří lepek – mazlavou hmotu, která může způsobovat zhoršení střevní peristaltiky a snížené využívaní živin z krmné dávky. Zejména u plemene Irský setr se můžeme setkat s glutenovou enteropatií. je to vzácné vrozené onemocnění, projevující se intolerancí glutenu, částečnou atrofií klků, sníženou aktivitou enzymů a rozvojem malaabsorpčního syndromu.
Zdroj tuků
Při onemocnění GIT je potřeba podávat pacientům krmivo s redukovaným obsahem tuků (11 – 15% a méně celkového tuku). Příjem krmiva s vysokým obsahem tuku je kontraindikován u zvířat s EPI, postakutní pankreatitidou a lymfangiektázií. Nevstřebaný tuk je střevními bakteriemi metabolizován na hydoxy mastné kyseliny. Navíc tyto bakterie dekonjugují žlučové kyseliny. To všechno vede k sekrečnímu průjmu z distální části tenkého střeva a kolonu.
Zdroj vlákniny
Vláknina je fermentována střevními bakteriemi za vzniku významných konečných produktů, a to kyseliny octové, propionové a máselné (těkavé mastné kyseliny). Tyto kyseliny slouží jako energetický zdroj pro kolonocyty. Uhrazují více než 70% jejich energetických potřeb. Navíc přítomnost těchto kyselin v kolonu výrazně zvyšuje mitotický potenciál kolonocytů. Tím dochází k rychlejší obnově buněk. Průměrně se buňky obnovují po třech dnech. Také krevní tok v kolonu se v přítomnosti těchto kyselin zvyšuje. Substráty, které jsou nejméně fermentovatelné a jejichž fermentací vzniká nejméně těkavých mastných kyselin jsou například celuloza, burákové slupky, metylceluloza a další. Přesně opačný efekt mají tyto látky – guarová guma a pektin. Středně fermetovatelné jsou řepná pulpa, inulín, rýžové otruby a arabská guma. Vláknina zvyšuje peristaltickou aktivitu v distální části tenkého střeva, zatímco peristaltickou aktivitu kolonu pravděpodobně snižuje.
Celkově vláknina působí jako preventivní prostředek proti průjmu. Zvyšuje absorpci sodíku ve střevě, napomáhá zachovávat elektrolytovou a vodní rovnováhu a poskytuje živnou půdu pro růst prospěšných střevních bakterií zatímco inhibuje proliferaci těch patogenních.
Diety navržené na zvládnutí střevních potíží by měly obsahovat mezi 3 – 7% vlákniny, ale ne více než 10%. Rychlá fermentace a nadměrná tvorba těkavých mastných kyselin může způsobit řídkou stolici nebo průjem. Navíc vznikající plyn může zhoršit trávení a absorpci nutrietů krmiva.
Jako prebiotika označujeme nestravitelné komponenty krmiva, které příznivě působí na organismus. Mechanismus jejich účinku spočívá v tom, že podporují aktivitu a růst selektivních kmenů bakterií v tlustém střevě. Nejvíce prebiotik jsou po chemické stránce sacharidy s krátkým řetězcem např. inulín, galaktoologosacharidy, laktuloza, fruktooligosacharidy (FOS) a mananooligosacharidy (MOS). FOS a MOS jsou vysoce fermentovatelné prebiotika. MOS jsou obsaženy v kvasnicích. Působí tak, že zabraňují přichycení a kolonizaci patogenních bakterií na stěnu střevních buněk. FOS můžeme najít v ovoci, zelenině a obilovinách. Koncentrovaným zdrojem FOS jsou slupky ze sojových bobů, psyllium, čekanka a kořen cukrové řepy. V současné době je možno FOS vyrábět i komerčně fermentací substrátu plísní Aspergilus niger. FOS jsou selektivně metabolizovány bakteriemi rodu Bifidobakterium, Lactobacillus a Bacteroides. Tyto bakterie utilizují FOS přednostně před glukozou jako zdroj energie. Zatímco škodlivé bakterie jako Eubakterium, Salmonella a Clostridium FOS neutilizují vůbec nebo s menší efektivností. Prebiotika můžou pomoci zvládnout taková onemocnění jako SIBO/ARD a přerůstání střeva patogenními bakteriemi. Existují důkazy, že podávání prebiotik laktujícím fenám má vliv na množství imunoglobulinů v jejich mléce a zdraví sajících štěňat.
Jako probiotika označujeme prospěšné živé mikroorganismy osídlující trávicí trakt lidí i zvířat. Udržují vybalancovanou a zdravou střevní mikrobiální populaci. Působí jako prevence stresových, infekčních a s antibiotiky asociovaných průjmů, mají pozitivní vliv na GIT při SIBO a IBD. V současné době jsou probiotika dostupná v celé řadě forem – jako pasta, roztok, tablety atd. Je vhodné je při podávání zamíchat do předkládaného krmiva.
Směs probiotik a prebiotik se označuje jako symbiotikum.
Hepatobiliární onemocnění
Pro diagnostiku patologií jater a žlučových cest máme celou řadu metod. Mezi nejpoužívanější z nich můžeme zařadit analýzu krve a to jak hematologickou (PT, APTT, počet destiček) tak hlavně biochemickou (ALT, AST, ALP, GGT, žlučové kyseliny). Jako další metody můžeme použít analýzu moči, zobrazovací metody, a jaterní biopsii. Stimulační test žlučových kyselin je nejvíce specifický a senzitivní pro detekci hepatobiliárních onemocnění. Zvíře necháme před testem 12 hodin hladovět, poté odebereme krevní vzorek, podáme zvířeti krmivo a po dvou hodinách opět odebereme vzorek krve.
Léčba onemocnění jater
Pro léčbu onemocnění jater se využívá celá řada látek, které mají buď zabránit nenávratným změnám v podobě fibrotizace nebo látky, které mají povzbudit hepatocyty k množení. Glukokortikoidy se využívají při chronické hepatitidě. Využívá se jejich protizánětlivého a protifibrotického účinku. Glukokortikoidy jsou kontraindikovány v konečném stadiu cirhozy jater, při fibroze nezánětlivé etiologie a u pacientů s výraznou portální hypertenzí.
Při onemocnění způsobené bakteriální infekcí je nasnadě nasadit vhodná antibiotika. Látky s protifibrotickým účinkem se používají v konečném stadiu všech chronických jaterních onemocnění. Fibroza je nevratný proces poškození jater. Kolchicin, alkaloid z ocúnu jesenního, se používá pro svou schopnost zastavit a redukovat fibrotizaci jater (zastavuje množení fibrocytů a stimuluje kolagenázovou aktivitu). Jako vedlejší efekt se však dostavuje zvracení a průjem. Ursodeoxycholová kyselina (UDCA) je netoxická žlučová kyselina, která zvyšuje tok žlučových kyselin, rozřeďuje toxické žlučové kyseliny a moduluje imunitní systém. Je kontraindikována při obstrukci žlučovodů. Další látky používané při onemocnění jater jsou například Azathioprine, S-Adenosyl-L-Methionin (SAMe), Silymarin a dieta.
Glutathion (GSH) je jednou z hlavních defenzních látek v hepatocytech. Glutathion je tripeptid složený z kyseliny glutamové, cysteinu a glycinu. Chrání hepatocyty před intoxikací. Nedostatek glutathionu způsobuje oxidativní stres. SAMe je prekurzorem cysteinu, jedné ze základních aminokyselin v molekule glutathionu. Zvířatům se podává pouze po předchozím nakrmení.
Mezi hlavní účinky SAMe patří zvýšená hladina GSH v játrech, stimulace buněčné replikace a reparace, ochrana jaterních buněk před toxiny a buněčnou smrtí a podpora proteosyntézy. Navíc působí jako ochrana před volnými radikály, stabilizuje buněčnou membránu erytrocytů a u koček zlepšuje odtok žluči.
Sylimarin je složka extrahovaná z plodů rostliny Ostropestřec mariánský (Silybum marinum). Sylibin je jeho nejaktivnější součástí. Působí jako velmi silný lapač volných radikálů díky zvýšení intracelulární hladiny enzymu superoxiddismutázy (SOD).
Dieta při hepatobiliárních onemocněních
Energie
Druh a závažnost jaterního onemocnění má značný vliv na energetické nároky pacienta. Proto musí být dietní režim individuálně přizpůsoben nárokům jednotlivého pacienta. U pacientů s akutním zánětlivým onemocněním jater probíhají katabolické reakce více než u pacientů s cirhózou. Z toho důvodu jsou jejich nároky na energii vyšší.
Nemocná játra mají sníženou kapacitu pro skladování sacharidů a utilizaci proteinů. Z toho důvodu je vhodné podávat potravu častěji po malých dávkách. Zlepší se tím dostupnost sacharidů a rovnováha dusíku v těle.
Proteiny
Zvýšené dávky proteinů v krmné dávce k udržení pozitivní dusíkové bilance je třeba dodávat pacientům uzdravujícím se z ischemického poškození jater, akutní nekrózy jater a pacientům s chronickou hepatitidou.
Zvířatům s těžkým poškozením jater je třeba podávat dietu se sníženým množstvím proteinů. Minimální příjem proteinů pro zdravého psa je 1,25-1,75 g/kg.ž.hm., pro psa s chronickým selháním se toto množství pohybuje v rozmezí 2,0-2,2 g/kg.ž.hm. Toto množství vysoce kvalitního proteinu poskytne 70 – 110 kcal/(kg z d).
Restrikce proteinů u kočičích pacientů by neměla překročit minimální hodnoty doporučované pro kočky s chronickým ledvinným selháním. 3,3 – 3,5 g/kg.ž.hm. vysoce hodnotného proteinu v krmivu poskytne 70 – 80 kcal/(kg z d). Kočky nejsou schopné efektivně šetřit dusíkaté látky po restrikci.
Protein restrikční diety nejsou vhodné pro kočky s lipidózou jater a chronickou cholangiohepatitidou.
Vysoký obsah tuku v dietě a snížené množství proteinů jsou často nesprávně doporučovány u psů s vakuolární hepatopatií. Vakuolární hepatopatie je onemocnění způsobené zvýšeným ukládáním tuku v játrech bez schopnosti jeho transportu do periferií, kde může být oxidován. Toto onemocnění se vyskytuje u kníračů, šeltií, psů s pankreatitidou, IBD nebo cukrovkou.
Odhad proteinové a energetické malnutrice je založen na hodnocení změny tělesné hmotnosti, na hodnocení sérové koncentrace proteinů produkovaných játry ((albumin, a-globuliny, fibronektin, fibrinogen), na určení BSC a koncentrace kreatininu v seru.
Rovnováha mezi množstvím proteinu potřebného k dosažení pozitivní dusíkové bilance a množstvím proteinu, který vytváří vedlejší efekt – proteinová tolerance může být zvýšená přídanými medikamenty – orálně podávaná antibiotika – neomycin, metronidazol, laktuloza, neživočišný druh proteinu a dieta obohacená solubilní vlákninou.
Podtrhnuto sečteno, jaterní dieta by měla být hlavně chutná a měla by obsahovat protein vysoké biologické hodnoty. Dále by měla mít snížené množství sodíku a naopak zvýšené množství zinku a vitamínu K. Pokud nehrozí nebezpečí jaterní encephalopatie, není potřeba snižovat v krmné dávce množství proteinu.
Lipidoza jater u koček
Lipidoza jater je získané onemocnění způsobené zvýšenou akumulací triacyglycerolů v buňkách jater, při kterém nakonec dochází k porušení samotné funkce jater. Toto onemocnění se objevuje u koček ve středním věku, které mají nadváhu či jsou obézní. Onemocnění je vázáno na periodu částečného nebo úplného nechutenství (např. vyvolané stresem). Méně často se lipidoza vyskytuje jako sekundární onemocnění, například při IBD, cukrovce nebo onemocnění ledvin.
Etiologie
Cirkulující mastné kyseliny jsou transportovány do jater, kde jsou buď metabolizovány jako zdroj energie nebo přeměněny na triacyglyceroly. Tyto nově syntetizované TAG jsou z jater transportovány na bílkovinném nosiči (VLDL) do periferních tkání. Pokud dojde k překročení oxidační nebo transportní kapacity jater, rozvijí se lipidoza.
Kočky s lipidózou vykazují příznaky proteinové malnutrice (ztráta osvalení, anemie, hypoalbuminemie). Přidávání malého množství proteinů obezním kočkám během lačnění může sloužit jako prevence akumulace jaterních lipidů. Deficience argininu methioninu a L-karnitinu, sekundárně anorexie a ztráta proteinů usnadňují nástup FHL.
Klinické příznaky
K rozvoji onemocnění dochází po sedmi či více dnech nechutenství. Kočky najednou přestanou přijímat krmivo po náhlé změně životního stylu či prostředí nebo vlivem stresu – přestěhování do nového domu, příchod nového mazlíčka nebo změna krmiva. Později se objevuje deprese, ztráta hmotnosti, atrofie svalstva a žloutenka. Může se objevit i zvracení a průjem.
Laboratorní nálezy
Laboratorním vyšetřením krve se zjišťují zvýšené aktivity jaterních enzymů, bilirubinu a žlučových kyselin. Může také docházet ke zvýšení močoviny a amoniaku v krevní plazmě. Neregenerativní anemie je typická nepravidelnými tvary erytrocytů. Diagnoza by měla být potvrzena jaterní biopsií.
Léčba a dietární doporučení
Pro léčbu lipidozy je potřeba donutit pacienta přijímat krmivo a vodu. Násilné krmení může kvůli stresu při jeho provádění jen prohloubit nechutenství. Pokud není zbytí, je vhodné zavézt nasoesofageální sondu. Při prvním krmení za pomoci sondy je třeba kočce poskytnout čtvrtinu až polovinu její metabolizovatelné energie. Postupně se množství metabolizovatelné energie v krmné dávce zvyšuje. Krmivo bychom měli podávat minimálně 4krát denně. Jakmile se kočce vrátí apetit, můžeme snížit frekvenci krmení sondou a nechat kočku jíst samovolně. Je třeba minimalizovat veškerý stres, který může stav zvířete zhoršit.
Je třeba poskytovat krmivo, které obsahuje vysoké množství kvalitního proteinu a přiměřené množství tuku. Kočky, u kterých pozorujeme příznaky hepatoencephalopatií, krmíme nejdříve krmivem se sníženým obsahem proteinů. Jakmile odezní neurologické příznaky můžeme postupně dávky proteinů zvyšovat.
Většina koček potřebuje 3 až 6 týdnů intenzivní dietní terapie, poté se jejich laboratorní hodnoty obvykle vrátí do referenčního rozmezí.
Dieta předkládaná kočce s lipidózou by měla obsahovat ve vodě rozpustné vitamíny - zvláště thiamin, dále L-karnitin, taurin, vitamín E a vitamín K.
Pancreatitis - Zánět slinivky břišní
Akutní pankreatitida je většinou reversibilní krátce trvající onemocnění. Může mít extrémně rychlý nástup, ve vážných případech dochází k tkáňové nekróze a onemocnění může skončit potencionálně smrtí postiženého zvířete. Akutní forma onemocnění je nejčastěji diagnostikována u psů.
Chronická pankreatitida je trvalé, obvykle progresivní zánětlivé onemocnění. Je charakterizováno neustálým narušováním struktury a exokrinní (někdy i endokrinní) funkce žlázy. Povětšinou je diagnostikována u koček. Často probíhá jako subklinická nebo mírná forma onemocnění. Řada případů kvůli svému mírnému průběhu uniká diagnostice.
Mezi rizikové faktory, které jsou často zodpovědné za vznik pankreatitidy můžeme zahrnout nadváhu, obezitu, hyperlipidémii, krmení tučným krmivem, potravní intoleranci, přítomnost dalších onemocnění GIT (IBD, jaterní onemocnění), neoplastické procesy a expozice organismu účinkům léků (organofosfáty, L-asparagináza, azathioprin,…) nebo infekčních agens (Toxoplasma, FIP,…). Avšak řada případů je klasifikována jako idiopatická pankreatitida.
Klinické příznaky
Mezi hlavní klinické příznaky patří nechutenství, deprese, apatie, zvracení a ztráta hmotnosti. Dostavuje se také bolestivost břicha, dehydratace, ikterus a dušnost.
Management pankreatitidy
Zvířeti s pankreatitidou je nejdříve nutno zavést intravenozní kanylu a podat odpovídající množství tekutin. Pomocí infuzí se snažíme zkorigovat hypokalemii, elektrolytovou a acidobazickou rovnováhu. Na zmírnění bolesti je možno aplikovat opiáty.
Ve velmi akutních případech je možno zvážit krmení zvířete enterálně.
Dietní management pankreatitidy u psa
Při akutní pankreatitidě je vhodné v počátečních 48 hodinách nasadit psovi hladovku. Tím poskytneme odpočinek slinivce (snížení stimulace). Po této době je možno začít postupně předkládat krmivo, je –li tolerováno. Tuky a aminokyseliny jsou nutrienty, které zvyšují sekreci pankreatické šťávy. Proto z počátku zvolíme krmivo obsahující zvýšené množství sacharidů. Pak postupně zvyšujeme podíl tuků a proteinů v krmné dávce (z pravidla první a druhý týden po objevení se onemocnění).
Dietní management pankreatitidy u koček
Abdominální bolest a zvracení obvykle způsobují u koček nechutenství a následnou ztrátu hmotnosti. Dlouhodobé hladovění (více než 3 dny) sice zajistí uklidnění slinivky, ale prohlubuje ztrátu hmotnosti. Navíc hrozí riziko rozvoje jaterní lipidózy.
Pokud kočka netrpí zvracením, můžeme období nechutenství překonat pomocí gastrostomie nebo esofagostomie. Většinou jsou dobře tolerovány. Pro tento druh krmení můžeme použít komerční udržovací nebo intestinální dietu. Kočky jsou fyziologicky adaptovány na příjem krmiv s vysokým obsahem proteinů a tuků, tudíž jim toto krmení vyhovuje.
Exokrinní pankreatická insuficience
Slinivka břišní je žláza produkující jak pankreatickou šťávu (exokrinní funkce) tak hormony (endokrinní funkce). Nedostatečné množství trávicích enzymů se projevuje jako maldigesce a malabsorpční syndrom. U psů je častou příčinou EPI selektivní atrofie buněk acinů pankreatu. Byl zjištěn dědičný potenciál onemocnění. Nejvíce případů bylo diagnostikováno u Německých ovčáků a Kolií.
Méně často se EPI vyskytuje u koček jako následek chronické pankreatitidy. Genetický potenciál EPI u koček nebyl prokázán.
Hlavní enzymy jsou:
- Amyláza – enzym štěpící cukry (cukry a škroby v obilovinách, zelenině a ovoci)
- Lipáza – štěpí tuky
-Trypsin a proteázy štěpí bílkoviny na peptidy a aminokyseliny
Klinické příznaky:
Majitelé si často všimnou postupující ztráty hmotnosti i přes zachovalou chuť k jídlu. Zvířata častěji vylučují (někdy každou hodinu). Jejich výkaly jsou objemné, mastné a nažloutlé, připomínající kravské výkaly. Zvířata je často požírají. Postižení psi trpí nadýmáním a můžeme u nich slyšet kručení v břiše. V některých případech se může objevit vodnatý průjem nebo zvracení. Někteří psi však nevykazují žádné typické příznaky. SIBO/ARD je komplikací u více než 70% psů s EPI.
Dlouhodobý management EPI
Dlouhodobý management spočívá v podávání náhradních enzymů a v úpravě složení krmiva. Tato úprava podpoří trávení a vstřebávání živin. Podávané krmení musí být vysoce stravitelné. Z toho důvodu je lepší pokud je snížené množství vlákniny – podáváme krmivo bez obilovin. Navíc je vhodné krmivo obsahující hydrolyzovaný protein. Uvádí se, že stravitelnost by měla být vyšší než 90%. Předkládáme vyšší (1,5krát) množství krmiva, aby pacient nabral zpět ztracenou hmotnost. Krmivo má být energeticky bohatší, ale nemělo by obsahovat velké množství cholesterolu. Jsou vhodné mastné kyseliny se střední délkou řetězce. Pokud to není nezbytně nutné, nesnižujeme množství tuku v krmivu. U pacientů s EPI dochází často k deficinci vitamínů. Jedná se hlavně o kobaltamin, a vitamíny rozpustné v tucích. Sérová hladina vitaminu B12 by měla být pravidelně laboratorně zjišťována. Pacienti s fyziologickou hladinou B12 vitamínu v době stanovení diagnózy EPI obvykle v následujícím půl roce začnou být deficitní na tento vitamín. Pokud postiženému zvířeti nepodáváme B12, i přes zvládnutí EPI se rozvinou klinické příznaky nedostatku. Léčba spočívá v periodické injekční aplikaci kobaltaminu. Vyhneme se aplikaci multivitamínové směsi. Ta při aplikaci způsobuje bolest. Bylo zjištěno, že u některých pacientů dojde k rozvoji deficience vitamínů E a K i přes úspěšnou léčbu EPI pankreatickými enzymy. Přesný mechanismus tohoto jevu nebyl dostatečně vysvětlen.
Technika krmení spočívá v podávání malého množství krmiva několikrát denně (minimálně 3x). Navíc je třeba podávat antibiotika, za účelem zvládnutí SIBO.
Nalezení správné diety závisí na individualitě každého zvířete.
Enzymy
Enzymy podávané pro zvládnutí EPI se získávají extrakcí z prasečí slinivky. Enzymy v podobě prášku jsou účinnější než ve formě tablety.Počáteční dávky enzymů jsou docela vysoké. Obecně se používá 1 lžička enzymů v prášku na